歐盟醫療器械法規(MRD)給全球醫療器械制造商帶來了許多挑戰。其中之一就是對將在歐盟內開展貿易的所有醫療器械制造商的標簽要求產生重大影響。作為審核內容之一,標簽不規范對于取得MDR證書和對于在歐洲銷售醫療器械都有重大影響。
與 MDD 93/42/EEC 相比,歐盟 MDR 下的標簽需要更多信息,因為設備安全性和臨床有效性數據需要與用戶(醫務人員和患者/最終用戶)透明共享)。歐盟 MDR附件 I 第 III 章“一般安全和性能要求”中涵蓋了有關隨醫療器械提供的信息的所有要求。
根據歐盟醫療器械法規 (MDR)(第 2 條)中的定義,“標簽”是指出現在器械本身、每個單元的包裝上或產品包裝上的任何書面、印刷或圖形信息。多個設備。貼標簽過程的目的是識別醫療器械及其制造商,并傳達有關安全、使用和性能的基本信息。它適用于醫療設備的用戶,包括專業人士和消費者,以及相關第三方。
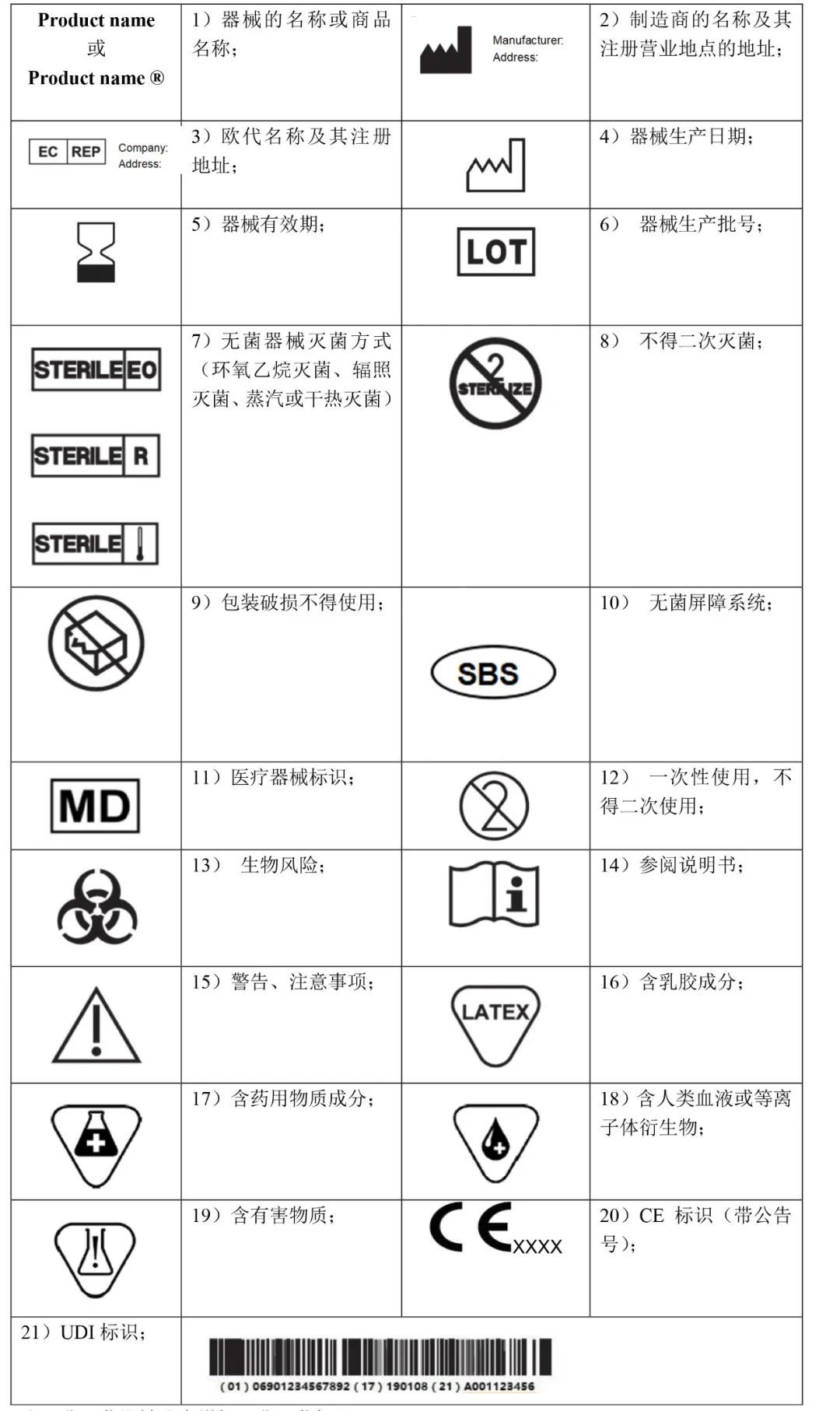
MDR 附錄I中第III章23.2對于產品標簽要求必須注明:
(a) 器械的名稱或商品名稱;
(b) 使用者識別器械所必需的詳細信息、包裝內容以及對于使用者不明顯的器械預期用途;
(c) 制造商的名稱、注冊商號或注冊商標及其注冊營業地點的地址;
(d) 授權代表的姓名和授權代表的注冊營業地點地址(若制造商在歐盟以外有其注冊營業地點);
(e) 若沒有指明可安全使用的日期,則指明制造日期。若日期清晰可辨,制造日期可作為批號或序列號的一部分。
(f) 指明適用的任何特殊儲存和/或處理條件;
(g) 若以無菌方式提供器械,還應指示其無菌狀態和滅菌方法;
(h) 需要立即引起器械使用者和任何其他人的注意、需要采取的警戒或預防措施。
(i) 若器械用于一次性使用,則相應指明。制造商的一次性使用指示應在整個歐盟內保持一致;
(j) UDI 載體應添加在該器械標簽和所有更大包裝上;
(k) 標簽應明顯、清晰和不可磨滅地添加在器械或其無菌包裝上。考慮到器械性質,無法或不適合將標簽添加到器械上時,應將 CE 標識添加在包裝上。CE 標識也應加貼在有使用明和任何銷售包裝中;
(l) 應采用器械上市國(同時也是成員國)指定的歐盟官方語言編寫,也可以采用預銷往國的當地語言;
(m) 標簽上所需的信息應在器械本身上提供。若不可行或不適當,則某些或所有信息可顯示在各單元的包裝上和/或多個器械的包裝上。
嘗試遵守歐盟 MDR 標簽要求時可能會遇到兩個問題。一是確保涵蓋所有必要的符號和信息。另一個是標簽的大小。由于需要更多的符號和數據,最大的挑戰將是如何將它們全部放在標簽上。在標簽設計過程中,請記住以下幾點:標簽和說明的媒介、格式、內容、易讀性和位置必須與預期用戶的技術知識、經驗、教育或培訓相匹配。此外,使用說明必須以預期用戶易于理解的術語編寫,并在適當的情況下補充附圖和圖表。
標簽可以以人類可讀的格式提供,并且可以用機器可讀的信息來補充。
微珂提供專業的MDR/IVDR認證服務,歡迎來電咨詢:
微珂醫藥擁有海內外專業成熟的技術團隊、以及與機構深度的戰略合作,服務于醫療器械企業,為企業提供優質的定制化服務,協助企業從產品技術要求編寫、產品檢測、臨床評價資料編寫與審核、申報與跟蹤,根據企業實際情況,進行質量管理體系建立,幫忙企業從管理到產品各環節一站式服務!
微珂集團服務熱線:4001182826!