臨近歲末,再次從加拿大衛(wèi)生部傳來喜訊,微珂助力國內(nèi)合作伙伴獲得一次性手術(shù)剪產(chǎn)品取得加拿大MDL證書,推動客戶產(chǎn)品進入加拿大市場!這也是本月的第二張加拿大MDL注冊證,從提交到批準,高效一次性審批通過。恭喜客戶產(chǎn)品獲批,預祝產(chǎn)品在北美市場大賣!
據(jù)海關(guān)數(shù)據(jù),2024年1- 6月,中國向加拿大出口醫(yī)療器械約28億人民幣,同比增長約22.06%;2024年1-6月,加拿大新增注冊醫(yī)療器械產(chǎn)品總計586款,其中112款為中國企業(yè)獲批。在此也特別提醒,加拿大衛(wèi)生部HC對于電商平臺上售賣醫(yī)療器械的實體要求提供MDEL注冊證書。


加拿大監(jiān)管當局
加拿大的監(jiān)管當局是Health Canada,所有進入加拿大市場的醫(yī)療器械和體外診斷器械都需要通過HC的申請許可才能進行上市。加拿大衛(wèi)生部下屬的Medica Devices Directorate是主要針對醫(yī)療器械的安全性和有效性進行審核評估的部門。
II、III、IV類器械加拿大申報的費用和審評周期一覽表
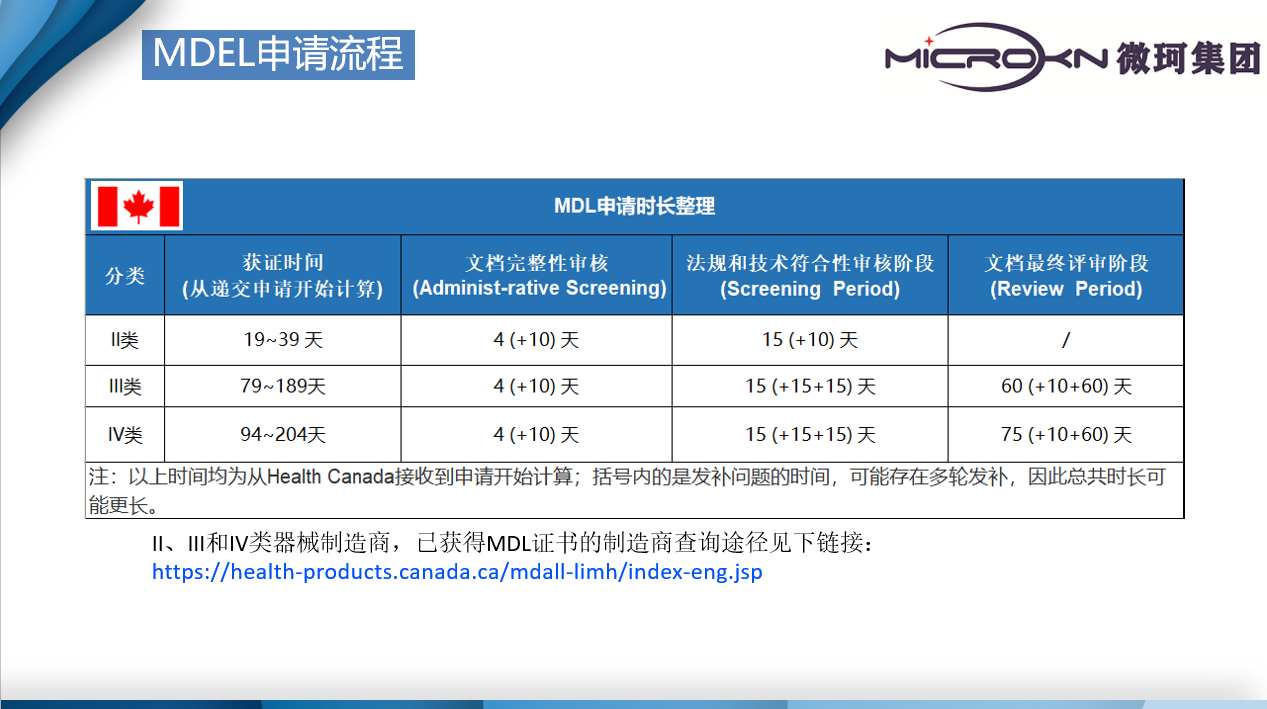
微珂可以為中國制造商提供加拿大一站式注冊,從MDSAP的咨詢輔導服務,到II/III/IV類器械的MDL注冊申報服務,還可以提供針對I類器械企業(yè)的MDEL注冊服務。
自2023年起,微珂在傳統(tǒng)的歐美注冊的優(yōu)勢下,陸續(xù)開發(fā)出了新項目方向,新項目方向主要面向的國家市場主要包括加拿大、澳洲、新加坡,印尼,馬來西亞,泰國,越南,菲律賓、沙特、巴西、俄羅斯、阿聯(lián)酋、墨西哥等國家和地區(qū)。截至目前,微珂已積累了豐富的全球注冊經(jīng)驗,產(chǎn)品風險覆蓋到各個風險類別,專業(yè)高效的服務深受客戶好評。
近年來,醫(yī)療器械出海備受越來越多國內(nèi)企業(yè)的關(guān)注,加拿大成為不少制造商的出海目標。微珂咨詢(Microkn)可提供的全球大多數(shù)國家的當?shù)刈浴H缒枰?a href="http://www.qingzhujituan.net.cn/list/21.html" target="_self">歐盟CE(MDR/IVDR)注冊服務,FDA注冊服務,加拿大MDL注冊,澳大利亞TGA注冊,MDSAP認證服務;及臨床實驗,臨床評價服務,專業(yè)的法規(guī)培訓服務,歡迎聯(lián)系微珂!