
IVDR的實(shí)施對(duì)整個(gè)行業(yè)和所有相關(guān)人員來(lái)說(shuō)是一項(xiàng)非常具有挑戰(zhàn)性的任務(wù):利益相關(guān)者、歐盟委員會(huì)和成員國(guó)。確保患者獲得安全有效的IVD是實(shí)施工作的重點(diǎn)。為了應(yīng)對(duì)與實(shí)施IVDR有關(guān)的挑戰(zhàn),本文件重新評(píng)估了實(shí)施的優(yōu)先事項(xiàng),并提出了成員國(guó)和委員會(huì)服務(wù)的聯(lián)合計(jì)劃。
本文的主要目的是商定在短期內(nèi)將有限的資源集中在何處,以確保在申請(qǐng)日期前盡快交付。本文件中規(guī)定的優(yōu)先事項(xiàng)是基于公共衛(wèi)生、患者安全和透明度的目標(biāo)確定的,這些目標(biāo)是新立法的關(guān)鍵,也是利益相關(guān)者最迫切的需求。
本聯(lián)合實(shí)施計(jì)劃是MDCG(包括相關(guān)小組)在利益相關(guān)者的參與下審查的結(jié)果。該計(jì)劃已在2021年 5月28日的MDCG會(huì)議上原則上獲得批準(zhǔn)。除了確定優(yōu)先事項(xiàng)外,該計(jì)劃還將作為監(jiān)測(cè)其執(zhí)行情況的動(dòng)態(tài)文件。各項(xiàng)行動(dòng)的狀態(tài)和時(shí)間規(guī)劃將動(dòng)態(tài)更新,以反映工作進(jìn)展。
這些優(yōu)先事項(xiàng)分為A、B兩組:
l A組包括對(duì)設(shè)備進(jìn)入市場(chǎng)至關(guān)重要的行動(dòng)(那些與應(yīng)急計(jì)劃框架和公告機(jī)構(gòu)的有效性有關(guān)的行動(dòng));
l B組包括法案和指導(dǎo)文件,雖然不是強(qiáng)制性的,但將極大地促進(jìn)參與者的工作,以及指定歐盟高風(fēng)險(xiǎn)IVDs參考實(shí)驗(yàn)室。它們包括歐盟參考實(shí)驗(yàn)室的指定、通用規(guī)范、若干主題和標(biāo)準(zhǔn)的指導(dǎo)。
對(duì)于A組和B組,確定了列為優(yōu)先級(jí)別的行動(dòng)列表。其中我們篩選了正在進(jìn)行或者將要進(jìn)行的部分,與大家分享。
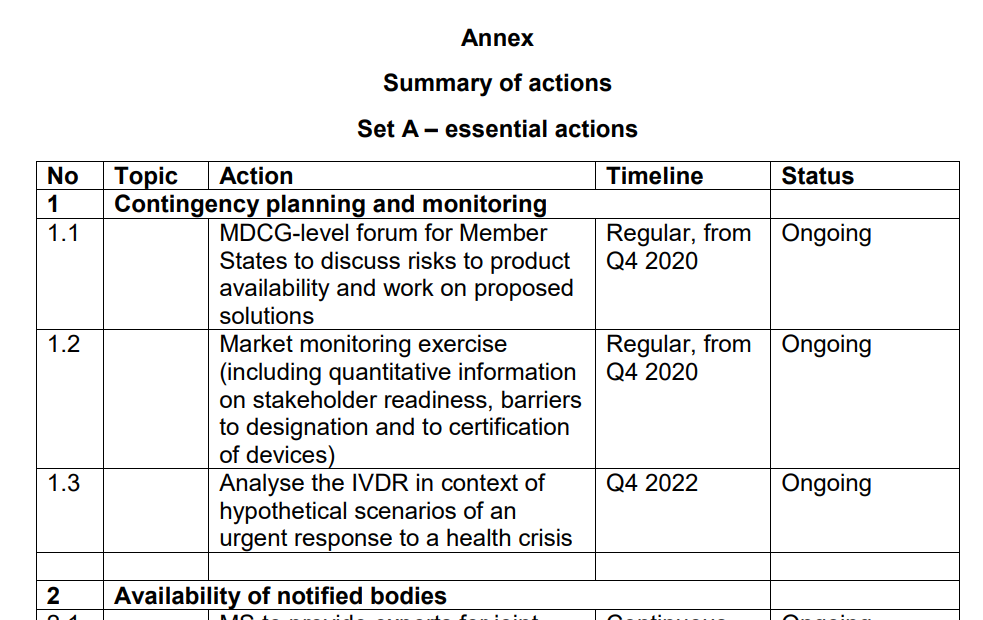
A組
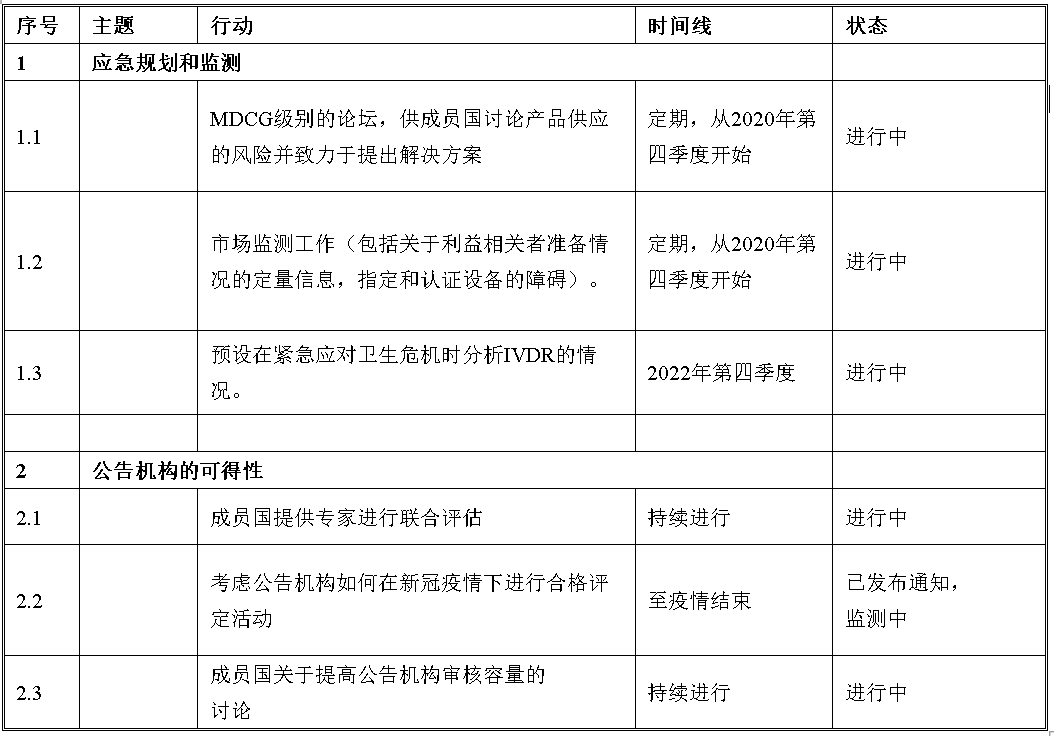
B組
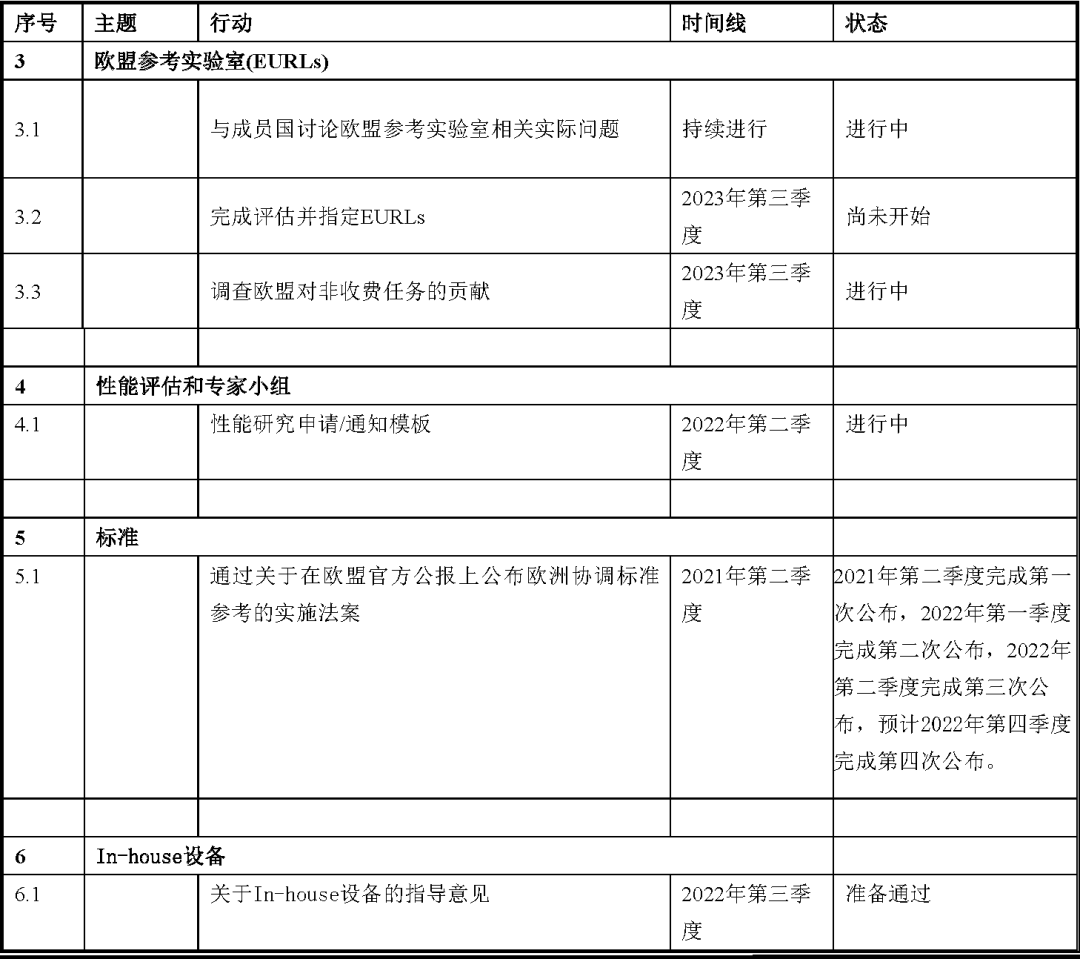
從上我們可以看到應(yīng)對(duì)IVD認(rèn)證產(chǎn)品供應(yīng)的風(fēng)險(xiǎn),以及可能出現(xiàn)的公共衛(wèi)生危機(jī)情況,關(guān)于提升公告機(jī)構(gòu)審評(píng)產(chǎn)能的討論將會(huì)持續(xù)進(jìn)行。在歐盟的官方公報(bào)上,更多的歐盟協(xié)調(diào)標(biāo)準(zhǔn)將會(huì)公布。歐盟高風(fēng)險(xiǎn)IVDs參考實(shí)驗(yàn)室的評(píng)定正在進(jìn)行。
微珂將持續(xù)關(guān)注IVDR實(shí)施推進(jìn)的動(dòng)態(tài),助力企業(yè)實(shí)施歐盟市場(chǎng)戰(zhàn)略。